PARP inhibitori: novi smjer u liječenju raka jajnika
Rak jajnika je i dalje vodeći uzrok smrti ginekoloških karcinoma u svijetu i jedan je od pet vodećih uzroka smrti od raka kod žena u Sjedinjenim Državama. Uz operaciju se liječenje sastoji od kombinacije kemoterapije platine i taksana koja ima visoku stopu dobrog odgovora; međutim, većina žena razvija trajnu ili recidivirajuću bolest.
Kliničke smjernice, objavljene od strane Društva za ginekološku onkologiju u listopadu 2014.g. navode da "žene s dijagnozom epitelnih ovarijskih, tubarnih i peritonealnih karcinomima trebaju dobiti genetsko savjetovanje i treba im biti ponuđeno genetsko testiranje, čak i ako nema obiteljske povijesti." Pacijentice bi trebalo informirati da ovo genetsko ispitivanje služi za prognozu, informiranje o osobnom i obiteljskom riziku od raka ali i kao pomagalo u odabiru novih terapijskih sredstava, posebno inhibitora Poly (ADP-riboza) polimeraze (PARP).
Genetska uključenost BRCA
Mali dio karcinoma jajnika se može pripisati genetskim mutacijama s približno 10% -15% slučajeva uzrokovanih mutacijama spolnih stanica BRCA1 i BRCA2. BRCA1 štetne mutacije imaju rizik za rak jajnika približno 39% -46%, a rizik za rak jajnika je oko 12% -20% kod bolesnica s BRCA2 štetnim mutacijama. Kao tumorski supresorski gen, BRCA je uključen u proces popravljanja DNA. Točnije, u homolognu rekombinaciju (oblik dvostrukog lančanog mehanizma popravljanja DNA). Dakle, stanice s neispravnim BRCA proteinima ne mogu popraviti oštećenja dvostrukog lanca (DSB) u DNA.
Homologni rekombinacijski put je složen i uključuje niz gena. Nedostaci u ovom putu pojačavaju osjetljivost na inhibiciju PARP. Tumori koji imaju disfunkciju u homolognom putu rekombinacije, ali ne sadrže mutacije u genu BRCA, klasificirani su kao tumori s ""BRCAness"".
Općenito, nasljeđe neispravnog BRCA1 ili BRCA2 alela (mutacija spolnih stanica) samo po sebi nije dovoljno da uzrokuje razvoj raka. Umjesto toga, kada drugi, funkcionalni alel postane nefunkcionalan, rak može nastati kroz akumulaciju mutacija u genetskom kodu.
Nadalje, bez obzira na status BRCA spolnih stanica, rak ima visoku stopu genetske mutacije. Kao posljedica stopa mutacije, tumori mogu razviti nepovratne promjene u BRCA1 ili BRCA2 genima (somatskoj mutaciji).
Mehanizam aktivnosti PARP inhibitora
Obitelj enzima PARP ima ključnu ulogu u popravku DNA i stabilizaciji ljudskog genoma kroz popravak jednolančanih lomova (SSB) u DNA. Inhibitori PARP su izvorno razvijeni kao kemosenzitizirajući agensi za druge citotoksične agense. Kasnije je otkriveno da su stanice raka jajnika kod mišjih modela koje su bile deficijentne u BRCA proteinima bile posebno osjetljive na inhibiciju PARP. Na kraju je klinička strategija razvoja započela primjenjivati PARP inhibitore kod odabranih bolesnica s BRCA mutacijama.
Kao što je ranije spomenuto, stanice deficijentne u tumorskim supresorskim genima (BRCA1 i BRCA2) nemaju sposobnost popravljanja DSB-a. Inhibiranje PARP enzima će zbog toga uzrokovati povećanje SSB-a. Tijekom replikacije stanica, ovi SSB-ovi se pretvaraju u DSB. Konačno, akumulacija DSB-ova dovodi do stanične smrti. Koncept da se ova dva nedostatka - koji su nepovezani - mogu kombinirati da induciraju staničnu smrt, opisan je kao sintetička letalnost.
Točan mehanizam kroz koji djeluju PARP inhibitori nije potpuno razumljiv; međutim, trenutno postoje četiri modela koji objašnjavaju kako PARP inhibitori potiču sintetičku letalnost. PARP inhibitori mogu blokirati mehanizme popravaka izrezivanja baze, zamijeniti PARP enzime na oštećenoj DNA, smanjiti afinitet funkcioniranja BRCA enzima na oštećenoj DNA i suzbiti nehomologni kraj spajanja mehanizama popravka.
FDA odobrila PARP inhibitore
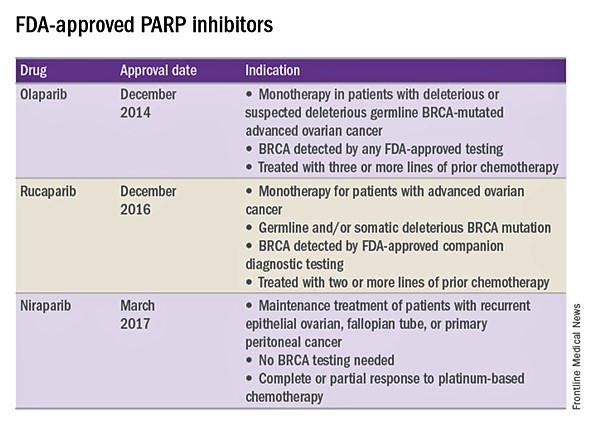
Posljednjih godina je Agencija za hranu i lijekove odobrila tri PARP inhibitora u liječenju raka jajnika u neznatno različitim kliničkim scenarijima.
Olaparib je testiran u pokusu od 193 bolesnica koje su imale rak jajovoda povezan s BRCA a koje su primile prethodne terapije.2 Ukupno je stopa odgovora u ovoj populaciji bila 41% (interval pouzdanosti od 95%, 28-54) sa srednjim trajanjem odgovora od 8 mjeseci. Ovi rezultati su doveli do toga da FDA odobri olaparib za liječenje raka jajnika kao četvrtu liniju terapije kod bolesnica s BRCA mutacijama.
Dva odvojena ispitivanja koja su koristila rucaparib su pokazala ukupnu stopu odgovora od 54% i trajanje odgovora od 9,2 mjeseci. 3,4 Ti raniji rezultati su omogućili da FDA napravi ubrzano odobrenje drugom PARP inhibitoru za uporabu kod karcinoma jajnika.
U novije vrijeme, faza III ispitivanja liječenja nirapariba u odnosu na placebo je uključila 553 žena s rekurentnim epitelnim rakom jajnika.5 Žene s mutacijama BRCA-linije koje su imale prvu liniju su imale interval od 21 mjesec bez ponovne pojave na niraparibu, u usporedbi sa 5,5 mjeseci kod onih na placebu. Čak i bez BRCA mutacija su žene imale interval od 9,3 mjeseca, u usporedbi s 3,9 mjeseci za placebo.
PARP inhibitori predstavljaju novu ciljanu terapiju za rak jajnika, osobito kod onih sa štetnim linearnim linijama ili somatskim BRCA mutacijama. U kombinaciji s genetskim testiranjem za BRCA mutacije, PARP inhibitori predstavljaju primjer prediktivnog biomarkera koji je uparen s prilagođenim terapijskim sredstvima. Podaci koji dospijevaju iz tekućih pokusa vjerojatno će proširiti mogućnost korištenja PARP inhibitora za liječenje raka jajnika.
Reference
1.
